광주과학기술원(GIST) 생명과학부
기능유전체학 연구실
박지환 (광주과학기술원(GIST) 생명과학부)
1. 연구실 개요
본 연구실의 연구 목표는 단일세포 오믹스 데이터를 통합 분석하여 다양한 만성질환의 병인을 이해하는 것이다. 모든 장기는 여러 종류의 세포로 구성되어 있고, 질병의 진행 과정에는 복잡한 변화가 수반되기 때문에 이를 단일 세포 수준에서 접근하는 것이 필수적이다. 그러나, 이전까지는 기술적인 한계로 여러 세포들의 집합체인 조직, 장기 수준의 연구가 이루어져 왔기 때문에 질병의 정확한 발생 과정을 이해하는 데 어려움이 있었다. 이러한 한계를 극복하기 위해 본 연구실의 핵심 기술인 단일세포 분석을 활용하여 기존의 한계를 극복하고 다양한 질병 모델을 연구하고 있다. 단일세포 분석을 통해 확인된 유전적 표적의 기저 분자 메커니즘을 동물 모델 연구 및 후성유전적 변형과 같은 기타 방법을 통해 연구하고 검증하고 있다.
2. 주요 연구 내용
(1) 단일세포 분석을 통한 만성질환의 이해
인체 내 장기와 조직들은 각각 특정 속성과 기능을 가진 수많은 세포 유형으로 구성되어 있다. 단일세포 전사체 분석은 유전자 발현 패턴을 기반으로 희귀 세포 유형을 포함하여 조직의 여러 세포 유형을 구별할 수 있다. 단일세포 전사체 분석은 조직에서 분리하기 어려운 세포 유형을 분석하고 다른 조건에서 샘플 간의 세포 유형 조성을 비교할 수 있다. 이를 통해 질병 샘플에서만 검출되거나 질병 관련 유전자가 특이적으로 발현되는 세포 유형을 확인할 수 있다. 각 세포 유형에서 질병에 따른 유전자 발현의 변화를 확인하는 것도 가능하다.
복잡한 질환의 경우 질병의 진행과 치료에 대한 반응이 환자마다 다르다. 또한, 정상 세포, 질병 세포 및 종양 환경은 개인의 조직 내에서 복잡한 상호 작용을 하여 종양 세포 특이적 치료를 어렵게 만든다. 단일 세포 해상도를 통해 개별 세포에서 돌연변이, 복제 수 변경 또는 바이러스 게놈을 식별할 수 있으므로 동일한 샘플에서 정상 세포와 질병 세포 간의 유전자 발현을 자세히 비교할 수 있다. 이를 분석하면 정상 세포에 비해 질병 세포에서 과발현되는 유전자를 찾거나 질병 세포에서 핵심 전사 인자를 찾을 수 있다. 또한, 세포-세포 상호작용 분석을 통해 정상 세포, 질병 세포 및 미세 환경 간의 활성화 또는 억제된 수용체-리간드 상호 작용을 확인할 수 있다. 세포궤적 분석은 개별 세포들의 연속적인 변화 과정에 따라 세포를 정렬함으로써 질병 발생의 중간 상태에 있는 세포를 식별할 수 있으며, 질병 발달 과정에서 세포 변화의 중요한 조절 유전자를 밝힐 수 있다 (Kim and Park 2021 Korean J Intern Med).
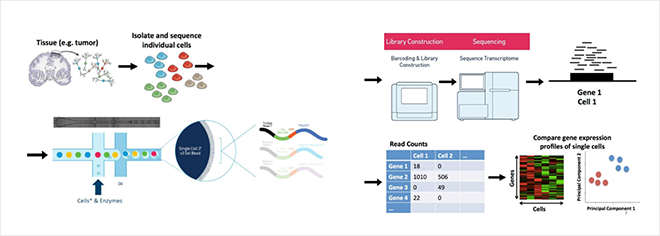 Figure 1. 단일세포 전사체 기술의 work flow
Figure 1. 단일세포 전사체 기술의 work flow
(2) 난치성암의 단일세포 분석을 통한 종양미세환경의 이해 및 핵심 유전자 발굴
단일세포 분석을 통해 난치성암의 종양미세환경에 대해 보다 정밀하게 분석하고 암의 진행단계 별 핵심 유전자를 동정할 수 있게 되었다 (Li et al. 2022 Military Medical Research). 예를 들어, 본 연구진은 갑상선암 중 가장 예후가 좋지 않은 미분화 갑상선암에 대한 단일세포 전사체 및 유전체 통합 분석을 통해 갑상선암의 진행과정을 추적하였으며, 그 결과 CREB3L1 전사인자가 암전이와 암세포 대사를 조절함으로써 미분화 갑상선암을 유도하는 핵심인자인 것을 밝혀냈다 (Luo et al 2021 Science Advances). 또한, 미분화 갑상선암이 진행될수록 종양 내 면역세포들의 면역억제 현상이 나타나 있음을 밝혀내기도 하였다. 향후 갑상선암의 종양과 종양주변 림프절의 비교분석을 통해 미세환경의 차이를 연구하고, 이를 통해 전이 기작을 밝혀내고자 한다.
이러한 단일세포 수준의 연구 방법론을 활용하여 본 연구진은 다양한 고형암에 대한 전체 암 (pan-cancer) 분석 연구를 수행하기도 하였다. 갑상선암, 췌장암, 간내담관암을 포함한 총 10종의 암종에 대해 226명 환자 샘플의 단일세포 전사체 데이터를 통합 분석하여 종양 내 암 연관 섬유아세포 (CAF: cancer associated fibroblast)의 다양성과 역할에 대해 제시하였다 (Luo et al. 2022 Nature Communications). 이와 같이 다수의 단일세포 전사체 데이터를 통합 분석함으로써 복잡한 질환을 보다 잘 이해할 수 있으며, 소수의 세포에 대해서도 시스템적 분석을 시도할 수 있다. 향후 암뿐만 아니라 다양한 질환에 대한 데이터를 수집하고, 나아가 인체 내 모든 세포에 대한 단일세포 전사체 거대 데이터베이스를 구축하여 정상 및 질병 세포를 보다 정밀하게 이해하고 마커를 동정하는 연구를 하고자 한다.
(3) 만성콩팥병의 단일세포 다중오믹스 분석을 통한 치료후보 발굴
만성콩팥병은 전세계적으로 열 명 중 한 명이 앓고 있을 정도로 흔한 질환임에도 불구하고, 아직까지 제대로 된 치료법이 없는 상황이다. 본 연구진은 만성콩팥병 동물모델, 신장 오가노이드의 단일세포 데이터와 환자의 전사체 데이터 통합 분석을 통해 만성콩팥병에서는 잘못 분화된 신장 내 근위 세뇨관 상피세포가 다수 존재하며, 이들의 지질대사 과정에도 문제가 생긴 것을 밝혀냈다 (Dhillon et al. 2021 Cell Metabolism). 이러한 근위 세뇨관 상피세포의 분화와 지질대사를 조절하는 핵심 조절인자가 에스트로겐 관련 수용체(ESRRA)이며, 이 유전자를 억제하거나 과발현 시킴으로써 만성콩팥병을 제어할 수 있다는 것을 확인했다.
한편, 만성콩팥병과 같은 만성질환은 만성적인 염증반응과 대사 과정의 변화에 따라 후성유전적 변화가 중요한 역할을 한다고 알려져 있다. 본 연구진은 당뇨병성 콩팥병 환자의 신장조직에 대한 단일세포 후성유전체 분석을 통해 다양한 세포종류에서 일어나는 후성유전적 조절에 따른 유전자 발현 조절 기작을 밝혀내는 연구를 수행하고 있다 (미출판 데이터). 또한 노화에 따른 콩팥내 긴길이 비번역 RNA (long non-coding RNA)의 발현 변화를 단일세포 수준에서 분석함으로써, 콩팥 노화에 따른 손상에서 긴길이 비번역 RNA 매개 후성유전적 변화를 연구하고 있다 (미출판 데이터). 향후 당뇨병성 콩팥병 진행 과정에서 사구체 내 세포들의 다이나믹한 변화에 대한 단일세포 분석, 루푸스신염에서의 면역 반응에 대한 연구로 연구 범위를 확장해 나갈 계획이다.
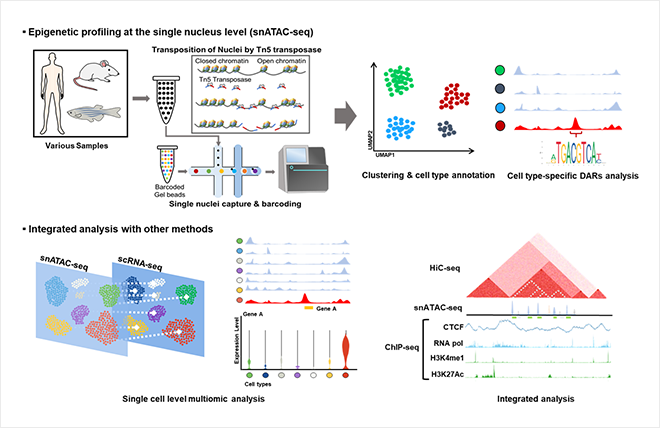 Figure 2. 단일세포 후성유전체 분석 기술 및 오믹스 데이터 통합 분석
Figure 2. 단일세포 후성유전체 분석 기술 및 오믹스 데이터 통합 분석
3. 맺음말
앞서 소개한 연구 외에도 본 연구실은 단일세포 분석 기술 개발 프로젝트도 수행하고 있다. 예를 들어, 단일세포 수준에서 전체길이의 유전자 분석을 통해 세포종류 별 유전자 선택적 스플라이싱 패턴과 돌연변이를 분석할 수 있는 기술, 특정 유전자 및 세포종류만 특이적으로 분석할 수 있는 단일세포 전사체 기술, 인체 조직 내에서 정상 발달 및 질병 진행과정에서 세포 계통을 단일세포 수준에서 추적할 수 있는 기술 등을 개발하고 있다. 이와 같이, 다양한 단일세포 수준의 데이터 통합 분석을 통해 보다 넓은 시야를 가지고, 보다 정밀하게 질병을 연구함으로써 앞으로 개인 맞춤형 정밀의료를 구현하는 데 도움이 될 수 있는 연구를 하고자 한다.
연구실 홈페이지: https://life.gist.ac.kr/genomics/index.do
 Figure 3. 2023년 GIST 기능유전체학 연구실 구성원
Figure 3. 2023년 GIST 기능유전체학 연구실 구성원
4. 대표논문