한국과학기술원 의과학대학원
대사비만당뇨 통합연구실
서재명 (KAIST)
연구실 개요
본 연구실은 2015년 카이스트 의과학 대학원에 대사비만당뇨 통합연구실(integrated lab of metabolism, obesity and diabetes)이라는 명칭으로 설립되었으며, 대사 현상의 조절 및 이와 관련된 과정을 이해하는 것을 목표로 한다. 주로 대사 항상성에 장애가 생긴 병리학적 상태(대사질환 및 노화과정)에서 이에 관여하는 지방조직, 근육, 뇌 등 다양한 장기에서의 분자생물학적 메커니즘과 치료 타겟에 관한 연구를 진행하고 있다. 특히, 많은 대사성질환은 비만에서 유래하는 경우가 많으나, 지방조직 자체를 근본적으로 제어하는 연구는 활발히 진행되고 있지 않다. 따라서 본 연구실에서는 비만 유래 대사성질환의 극복을 위해 근본 원인이 되는 백색지방조직의 생리학적 기능을 이해함으로써 대사성질환의 근원적 치료를 실현하는 원천기술을 확보하고자 노력하고 있다.
연구를 진행하기 위해 주로 마우스 모델을 적극적으로 활용하고 있으며, 이와 더불어 세포생물학 및 분자생물학적 기법 또한 활용하고 있다. 대사조절에 관여하는 여러 조직에서의 생리학적 기능과 대사질환의 연결고리가 되는 기전들을 밝히기 위해 단일세포 유전체 분석, 다중오믹스 기법 도입 등 다양한 실험적 접근을 시도하고 있으며, 국내/외 여러 기관과의 활발한 협업을 통해 비만, 당뇨와 같은 현대 난치병을 극복할 과학적 토대를 마련하기 위한 활발한 연구를 진행하고 있다.
주요 연구 내용
1) 백색지방조직에서 YAP-TAZ pathway의 생리학적 기능 연구
백색지방세포는 에너지 저장고로서의 역할을 한다고 알려져 있으며, 특히 지방세포 가소성의 적절한 조절은 지방 조직의 기능 유지와 전신 에너지 대사의 조율에 중요한 역할을 한다. Hippo 신호전달은 다양한 조직에서 조직의 크기를 조절하는 데 관여하는 것으로 알려져 있으나, 지방조직에서의 역할은 명확하지 않다. 본 연구실에서는 지방조직 특이적으로 LATS1/2 유전자를 결손시켜 YAP/TAZ pathway 활성을 유도한 모델을 통해 해당 pathway가 지방세포 가소성 조절 및 렙틴 발현에 중요한 조절인자로 작용하여 지방세포 탈분화 유도 및 에너지 소모율을 높이는 기전을 규명하였다. 나아가 현재는 해당 모델에서 나타나는 노화 관련 분비표현형(SASP) 증가, 단백질 분비 항상성 감소 및 섬유화 진행이 촉진되는 표현형에 주목하여 지방조직의 세포노화와 대사기능과의 관련성에 관한 연구를 진행하고 있다.
 그림1. 백색지방세포에서 YAP/TAZ 활성화에 의한 지방세포의 변화 연구
그림1. 백색지방세포에서 YAP/TAZ 활성화에 의한 지방세포의 변화 연구
2) FGF1에 의한 조직 및 에너지 항상성 조절 기전 연구
당, 지방 등 여러 형태의 에너지 섭취/저장과 소비의 균형을 유지하는 상태를 대사 항상성이라고 한다. 본 연구실에서는 지방조직, 시상하부, 근육 등의 주요 대사 중추에서 발현하는 FGF1(섬유아세포 성장인자1)이 조직 및 신체 에너지 항상성 조절에 있어 어떤 기능을 하는지에 관심을 갖고 연구를 진행하고 있다. 특히 FGF1은 당뇨 치료제 후보물질로서 활발한 연구가 되고 있으나, 이에 비해 조직 내재적인 FGF1의 역할에 대한 연구는 부족한 실정이다. 본 연구실에서는 (1)백색지방조직에서 PPARγ-FGF1 축이 지방세포 리모델링의 중요한 조절자로 작용하며 만성적인 대사 스트레스 및 급격한 영양 신호에 대응하여 대사 프로그램의 변화를 매개하는 역할과 (2)시상하부에서 발현하는 FGF1이 당 인식 뉴런에서의 혈당 상승 인식 조절 및 인슐린 신호전달과 독립적으로 렙틴 신호전달을 매개하여 당 대사 조절에 관여하는 역할에 대한 연구를 수행하고 있다.
 그림2. 지방조직 및 시상하부에서 FGF1에 의한 조직 및 에너지 항상성 조절 기전 연구
그림2. 지방조직 및 시상하부에서 FGF1에 의한 조직 및 에너지 항상성 조절 기전 연구
3) 조직 특이적 분비단백체 분석기법을 이용한 조직 간 crosstalk 연구
분비 단백체 표지-동정 기술(iSLET: in situ Secretory Protein Labeling via ER-anchored Turbo ID)은 특정 세포 내 ER 세포강 또는 엑소좀에서 신생합성-분비에 이르는 단백질을 바이오틴으로 표지하는 기술로, 기존 바이오틴 ligase의 표지 효율을 100배 이상 향상하여 생체 수준에서 단백질 표지 및 동정이 가능하다. 본 연구실에서는 해당 표지 인자를 발현하는 마우스를 제작하여 다양한 조직 특이적 cre 발현 마우스와의 교배를 통해 조직 특이적 표지-동정 가능한 모델을 수립하였다. 이를 활용하여 고지방식이, 인슐린 저항성 등 다양한 대사 스트레스 상황에서 특정 조직이 분비하는 분비단백체를 분석하여 ‘근원세포-순환경로-목적세포’를 규명하는 연구를 진행하고 있다.
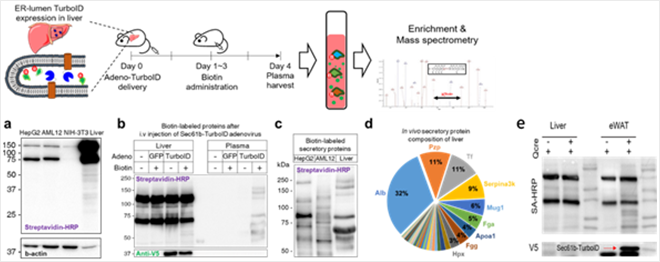 그림3. iSLET 기술을 이용한 간 특이적 분비단백체 검출
그림3. iSLET 기술을 이용한 간 특이적 분비단백체 검출
4) 미토콘드리아와 세포대사 및 갈색지방 기능 연구
미토콘드리아라는 세포소기관에서는 끊임없이 에너지(ATP)를 생산하여 세포의 생명 유지, 세포 대사 항상성 등의 중요한 역할을 한다. 본 연구실에서는 미토콘드리아 기능이 세포 대사 및 세포 정체성 조절에 작용하는 기전을 연구하고 있으며, 이와 관련한 질병 발병 기전에 큰 관심을 갖고 있다. 본 연구실에서는 고아 핵수용체(orphan nuclear receptor)의 하나인 ERRγ(Estrogen-related receptor γ)가 췌장 외분비선 선방세포의 세포대사와 세포 정체성을 조절하는 전사조절인자임을 규명하였으며, 나아가 췌장에서 발생하는 주요 질환인 췌장염과 췌장암의 발생에 관여하는 기전을 추가적으로 연구하고 있다.
에너지 발전소로서의 기능과 더불어 갈색지방에서의 미토콘드리아는 추위 자극에 반응하여 비떨림 열발생(nonshivering thermogenesis)이라는 작용을 통해 체온 조절에 중요한 역할을 하기도 한다. 본 연구실은 갈색지방에서 추위 자극이 가해졌을 때 (1) HuR이라는 RNA 결합 단백질이 미토콘드리아 OXPHOS 기능에 미치는 역할과 (2) Letmd1이라는 미토콘드리아 내막 단백질이 열 발생을 조절하는 기전을 연구하고 있다. 이러한 갈색지방 열 발생에 관한 기전을 이해하여 비만 치료 타겟으로 갈색지방의 활용 가능성 또한 모색하고 있다.
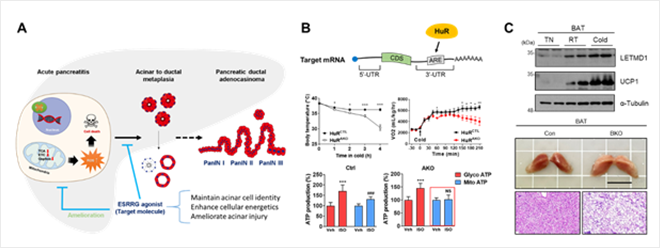 그림4. 미토콘드리아와 세포 대사 및 갈색지방 기능 연구
그림4. 미토콘드리아와 세포 대사 및 갈색지방 기능 연구 맺음말
연구실에서 진행 중인 다양한 연구들 외에도 본 연구실은 의과학대학원, 생명과학과의 다른 연구실 및 타 기관과의 공동연구를 활발히 수행하고 있으며, 보다 넓은 시각에서 대사 스트레스 상황에서의 병리학적 기전 규명 및 신체 대사 항상성을 바라보려는 노력을 하고 있다. 최근에는 새롭게 다년간의 대사 연구 경험을 바탕으로 백색지방조직의 노화 제어를 통한 대사성질환 치료기술 개발을 시도하고 있다.
본 연구실은 현재 지도교수인 서재명 교수와 연구교수인 강두석 교수, 신혜미, 박근영 박사후연구원, 사공용, Deniz Song 박사과정 학생 및 김택민, 이상헌, 이민홍, 이희라, 장애원 석박통합과정 학생들로 구성되어 대사질환 및 대사 항상성에 관한 연구를 진행하고 있다.
연구실 홈페이지 : https://imodkaist.wixsite.com/home
 그림4. 2023 대사비만당뇨 통합연구실 구성원 단체사진
그림4. 2023 대사비만당뇨 통합연구실 구성원 단체사진